国产三类医疗器械注册
- 服务详情

根据《医疗器械监督管理条例》(国务院令第650号)的规定,对医疗器械按照风险程度实行分类管理。第Ⅲ类是具有大风险,需要严格控制管理以保证其安全、有效的医疗器械,境内生产企业需要在所在地省(直辖市)药监局进行注册。
道和思源能够为客户在最短时间内克服医疗器械注册的技术困难,在满足医疗器械法规要求的前提下,帮助客户合理规避风险点,节省前期的项目成本及时间投入。道和思源为客户提供:
1.厂房分区指导及体系建立
2.样品及送检材料的准备(包括技术要求撰写)
3.产品检测
4.临床评价
5.注册资料的撰写及审核
6.注册递交及跟进
7.现场考核
8.生产许可
延续注册/登记事项变更/许可事项变更:
有效期届满需要延续的,医疗器械经营企业应当有效期届满6个月前提出延续申请。 有效期少于6个月仍需继续经营的,按照《医疗器械经营许可》新办办事指南递交材料,并提交原许可证正副本原件。 同时变更的,需附变更材料一套,变更材料见变更办事指南。
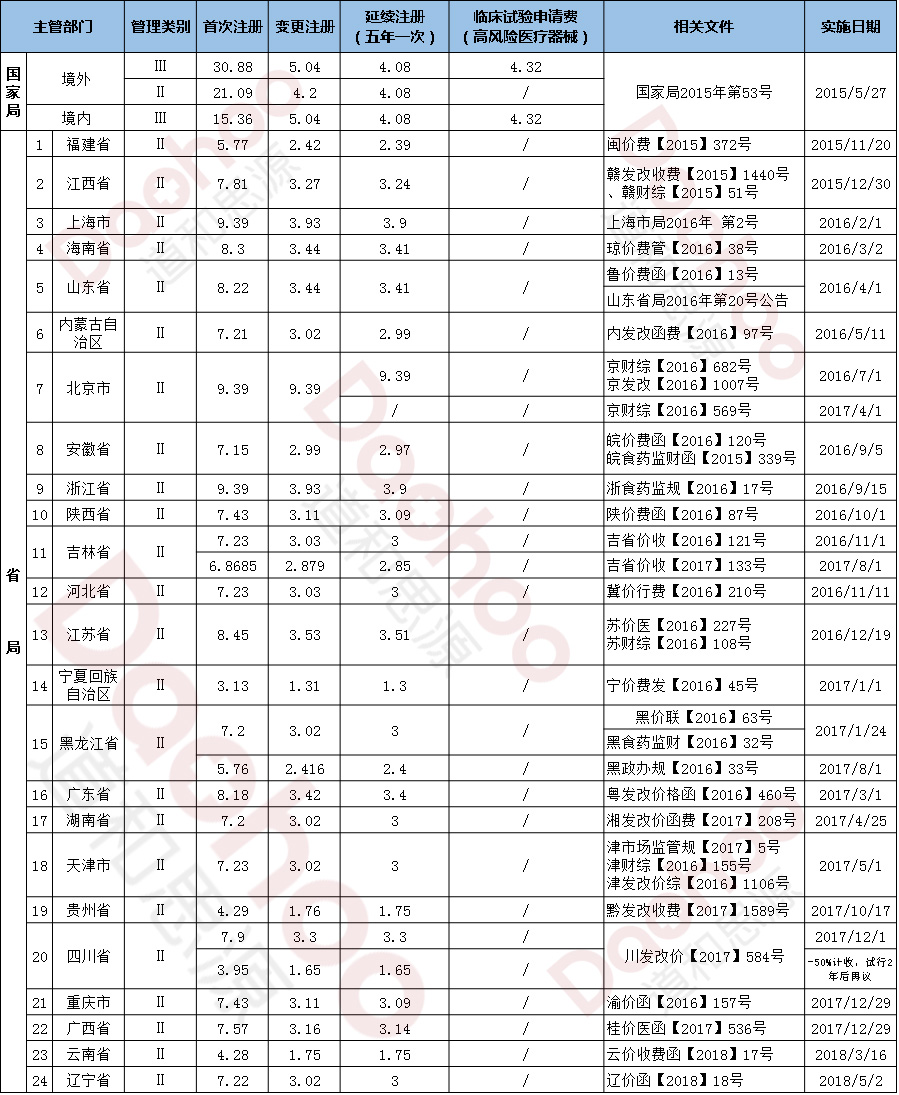
此项服务根据客户的需求定制注册方案,因产品不同、目的不同,研究复杂程度及规模差异很大,请留下您的联系方式,或者直接拨打电话13521090701(微信同号)。
服务流程:
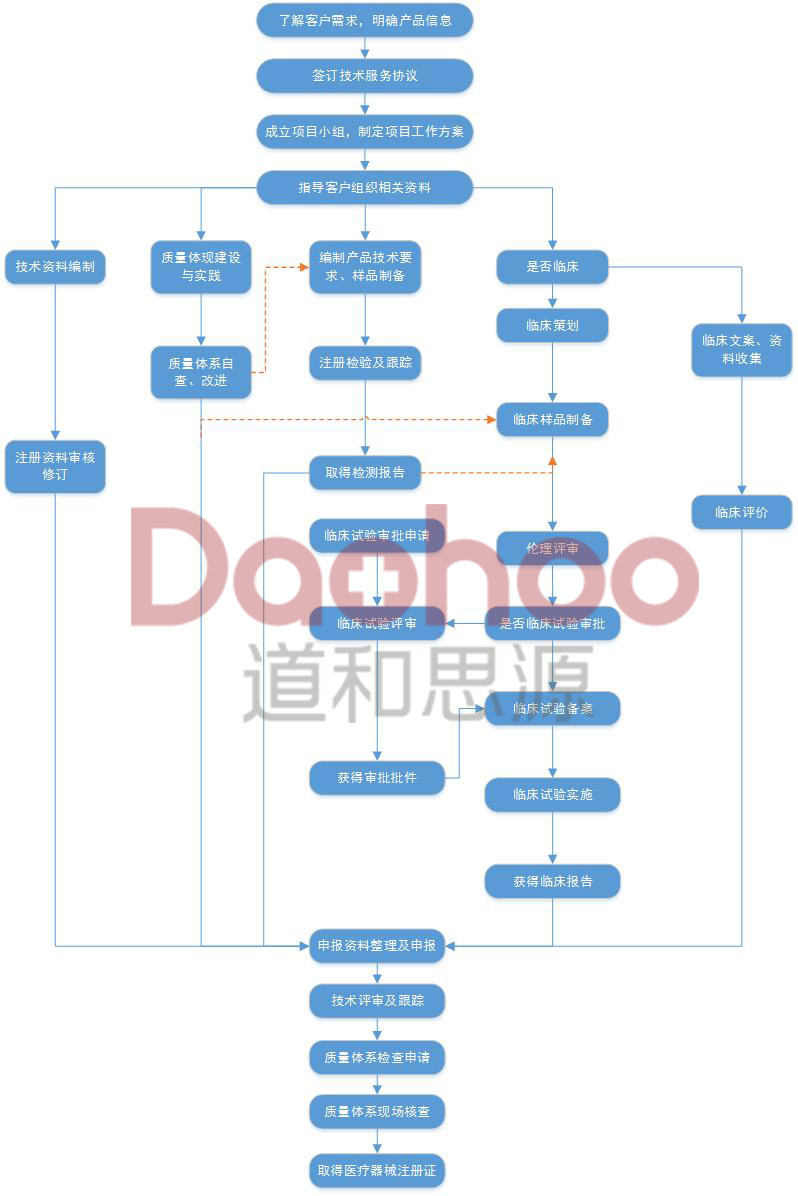
我们的服务优势

医疗器械合规上市,我们更快
快速响应、专业系统、快速行动、高效上市,道和思源首创的X7提速体系,使每个项目平均省时60天。

道和思源历史通过率100%
在全球服务的100+项目中,通过率100%。选择我们,就等于选择了竞争优势。

全程168步省心服务优化
关于于医疗器械合规上市相关法规、政策,我们更专业。关于合规上市的客户服务,我们更用心。




