三类医疗器械注册
- 服务详情

1、申请条件(进口、国产都适用)
(1)属于第三类医疗器械产品目录的产品(2014年第8号通告附件或已通过国家局分类界定后属于第三类医疗器械的产品(已录入国家局审批系统);
(2)办理第三类医疗器械注册申请事务的人员应当受生产企业委托,并具有相应的专业知识,熟悉医疗器械注册、注册相关的法律、法规、规章和技术要求;
(3)申请注册的第三类医疗器械,产品技术要求需符合{国家食品药品监督管理总局关于发布医疗器械产品技术要求编写指导原则的通告(第9号)};
(4)资料要求需符合(国家食品药品监督管理总局关于第三类医疗器械注册有关事项的公告)(第26号)的注册资料形式要求。
2、三类医疗器械首次注册
(1)建立体系
(2)体系内审
(3)体系运行
(4)体系模拟考核
(5)国家局申请
(6)CFDA签收/受理
(7)技术审评
(8)行政审评
(9)制证
3、三类医疗器械延续注册
(1)登记或许可变更
(2)修订技术要求
(3)产品注册检测
(4)CFDA签收/受理
(5)技术评审
(6)行政评审
(7)制证
4、三类医疗器械登记事项变更
(1)许可变更
(2)受理文件汇编
(3)原注册部门变更申请
(4)原注册部门签收/受理
(5)监督管理部门形式审查
(6)发给医疗器械注册变更文件
5、参考费用
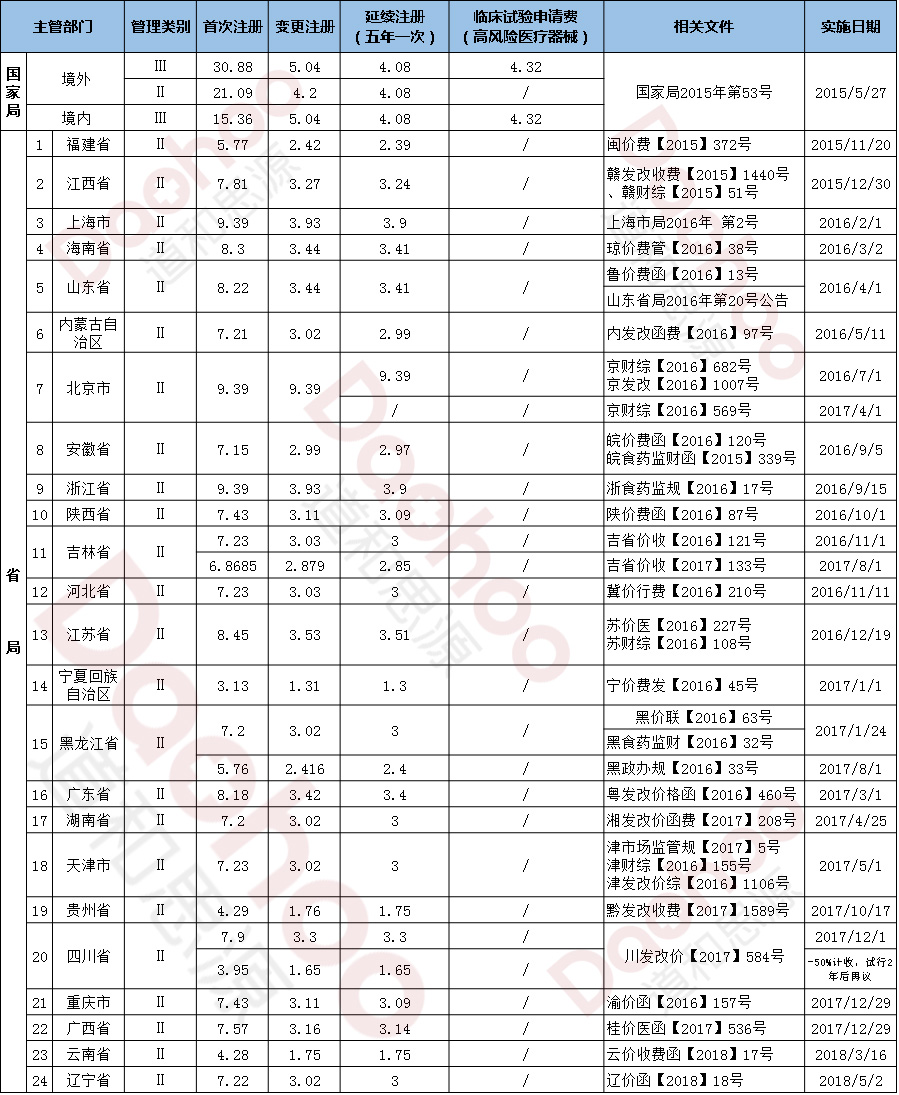
6、道和思源服务
三类产品备案保过体系和X7省时系统
三类产品备案资料的收集和评估
三类产品备案资料的撰写和符合
三类产品备案资料的递交
三类产品生产场地的注册
7、我们的服务优势

医疗器械合规上市,我们更快
快速响应、专业系统、快速行动、高效上市,道和思源首创的X7提速体系,使每个项目平均省时60天。

道和思源历史通过率100%
在全球服务的100+项目中,通过率100%。选择我们,就等于选择了竞争优势。

全程168步省心服务优化
关于于医疗器械合规上市相关法规、政策,我们更专业。关于合规上市的客户服务,我们更用心。
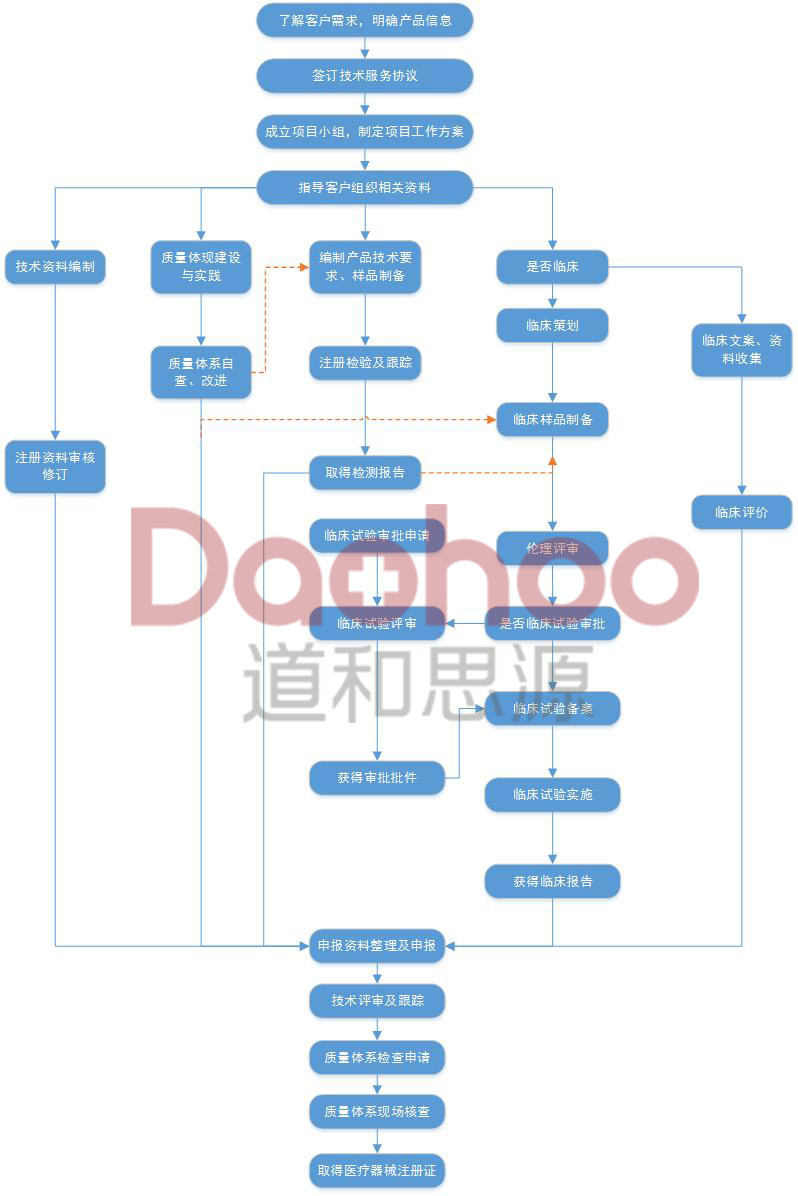
8、三类医疗器械注册服务流程