医疗器械注册证有效期为5年。有效期届满需要延续注册的,应当在有效期届满6个月前向原注册部门提出延续注册的申请。接到延续注册申请的食品药品监督管理部门应当在医疗器械注册证有效期届满前作出准予延续的决定。1、受理条件 申请事项属于本部门职权范围,申报资料齐全、符合形式审查要求。2、设定依据 1.《医疗器械监督管理条例》(国务院令 第680号)第十五条:“医疗器械注册证有效期为5年。有效期届...
医疗器械注册证有效期为5年。有效期届满需要延续注册的,应当在有效期届满6个月前向原注册部门提出延续注册的申请。接到延续注册申请的食品药品监督管理部门应当在医疗器械注册证有效期届满前作出准予延续的决定。
申请事项属于本部门职权范围,申报资料齐全、符合形式审查要求。
1.《医疗器械监督管理条例》(国务院令 第680号)第十五条:“医疗器械注册证有效期为5年。有效期届满需要延续注册的,应当在有效期届满6个月前向原注册部门提出延续注册的申请。除有本条第三款规定情形外,接到延续注册申请的食品药品监督管理部门应当在医疗器械注册证有效期届满前作出准予延续的决定。逾期未作决定的,视为准予延续。有下列情形之一的,不予延续注册:
(一)注册人未在规定期限内提出延续注册申请的;
(二)医疗器械强制性标准已经修订,申请延续注册的医疗器械不能达到新要求的;
(三)对用于治疗罕见疾病以及应对突发公共卫生事件急需的医疗器械,未在规定期限内完成医疗器械注册证载明事项的。”
2.《医疗器械注册管理办法》(国家食品药品监督管理总局令 第4号)第五十四条:“医疗器械注册证有效期届满需要延续注册的,注册人应当在医疗器械注册证有效期届满6个月前,向食品药品监督管理部门申请延续注册,并按照相关要求提交申报资料。除有本办法第五十五条规定情形外,接到延续注册申请的食品药品监督管理部门应当在医疗器械注册证有效期届满前作出准予延续的决定。逾期未作决定的,视为准予延续。”第五十五条:“有下列情形之一的,不予延续注册:
(一)注册人未在规定期限内提出延续注册申请的;
(二)医疗器械强制性标准已经修订,该医疗器械不能达到新要求的;
(三)对用于治疗罕见疾病以及应对突发公共卫生事件急需的医疗器械,批准注册部门在批准上市时提出要求,注册人未在规定期限内完成医疗器械注册证载明事项的。”
3.关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(国家食品药品监督管理总局公告 2014年 第43号 )附件5:医疗器械延续注册申报资料要求及说明
4.国家药品监督管理局关于修改医疗器械延续注册等部分申报资料要求的公告(2018年第53号)附件
3.1法定办结时限说明
1.受理:5个工作日,自受理之日起3个工作日内将申报资料转交技术审评机构。
2.审评:技术审评机构应当在60个工作日内完成第二类医疗器械注册的技术审评工作,应当在90个工作日内完成第三类医疗器械注册的技术审评工作。需要外聘专家审评、药械组合产品需与药品审评机构联合审评的,所需时间不计算在内,技术审评机构应当将所需时间书面告知申请人。质量管理体系核查的时间和申请人补充资料的时间,不计算在审评时限内,技术审评机构应当自收到补充资料之日起60个工作日内完成技术审评。
3.许可决定:20个工作日;
4.送达:10个工作日。
3.2承诺办结时限说明
1.受理:5个工作日,自受理之日起3个工作日内将申报资料转交技术审评机构。
2.审评:技术审评机构应当在60个工作日内完成第二类医疗器械注册的技术审评工作,应当在90个工作日内完成第三类医疗器械注册的技术审评工作。需要外聘专家审评、药械组合产品需与药品审评机构联合审评的,所需时间不计算在内,技术审评机构应当将所需时间书面告知申请人。质量管理体系核查的时间和申请人补充资料的时间,不计算在审评时限内,技术审评机构应当自收到补充资料之日起60个工作日内完成技术审评。
3.许可决定:20个工作日;
4.送达:10个工作日。
1.受理
申请人向国家药品监督管理局行政受理服务大厅提出申请,受理人员根据申报事项按照 《国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》(2014年第43号)、《食品 药品监管总局关于印发境内第三类和进口医疗器械注册审批操作规范》(食药监械管〔2014〕208号)的要求对申报资料进行形式审查。
申请事项属于本部门职权范围,申报资料齐全、符合形式审查要求的,予以受理;申报资料存在可以当场更正的错误的,允许申请人当场更正;申报资料不齐全或者不符合形式审查要求的,在5个工作日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申报资料之日起即为受理;申请事项不属于本部门职权范围的,即时告知申请人不予受理。
2.审查
受理人员自受理之日起3个工作日内将申报资料转交技术审评机构。技术审评机构应当在60个工作日内完成第二类医疗器械注册的技术审评工作,应当在90个工作日内完成第三类医疗器械注册的技术审评工作。需要外聘专家审评、药械组合产品需与药品审评机构联合审评的,所需时间不计算在内,技术审评机构应当将所需时间书面告知申请人。技术审评过程中需要申请人补正资料的,技术审评机构应当一次告知需要补正的全部内容。申请人应当在1年内按照补正通知的要求一次提供补充资料。技术审评机构应当自收到补充资料之日起60个工作日内完成技术审评。质量管理体系核查的时间和申请人补充资料的时间,不计算在审评时限内。
3.许可决定
国家药品监督管理局医疗器械技术审评中心应当在技术审评结束后20个工作日内作出决定,对符合安全、有效要求的,准予注册。对不予注册的,应当书面说明理由,并同时告知申请人享有申请复审和依法申请行政复议或者提起行政诉讼的权利。
4.送达
自作出审批决定之日起10个工作日内,国家药品监督管理局行政事项受理服务和投诉举报中心将行政许可决定送达申请人。
1.申请表
2.证明性文件
3.关于产品没有变化的声明 注册人提供产品没有变化的声明
4.原医疗器械注册证及其附件的复印件、历次医疗器械注册变更文件复印件
5.产品检验报告
6.符合性声明
7.其他
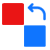
进口第三类医疗器械延续注册费:4.08万元;进口第二类医疗器械延续注册费:4.08万元
家发展改革委《关于重新发布中央管理的食品药品监督管理部门行政事业性收费项目的通知》(财税〔2015〕2号)和《关于印发〈药品、医疗器械产品注册收费标准管理办法〉的通知》(发改价格〔2015〕1006号),《国家食品药品监督管理总局关于发布药品、医疗器械产品注册收费标准的公告》(2015年第53号)。
医疗器械注册证有效期届满需要延续注册的需要何时提出申请?
答: 依据《医疗器械注册管理办法》(总局令第4号)第五十四条的相关要求:医疗器械注册证有效期届满需要延续注册的,注册人应当在医疗器械注册证有效期届满6个月前,向食品药品监督管理部门申请延续注册申请,并按照相关要求提交申报资料。